SAIBA MAIS SOBRE....
Óleo no macarrão, eis a questão

Leite derramado

Ovo cozido

A Fruta depois de cortada escureceu
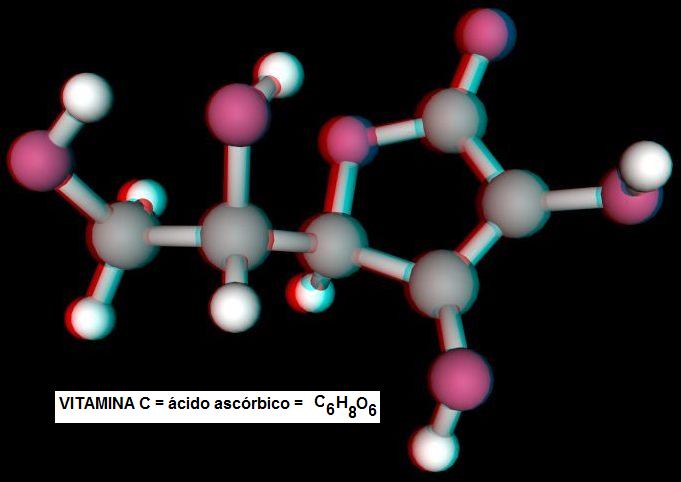
O que acontece: Você corta a maçã, a banana ou a ameixa e, minutos depois, as frutas escurecem e ficam nada apetitosas.  Como evitar: Jogue ácido. Limão ou laranja têm ácido ascórbico, C6H8O6(estrutura abaixo), que retarda a ação das enzimas e age como antioxidante. Não quer que suas frutas fiquem com gosto de limão? Compre vitamina C na farmácia e salpique por cima. Dá na mesma. .jpg) |
|---|
Cru e o Cozido
Entenda o que os 3 pontos do cozimento querem dizer, cientificamente é claro! MALPASSADO Temperatura no interior da carne: 50ºC Características: Carne fica opaca e de cor vermelha intensa, libera muito líquido e as proteínas começam a coagular AO PONTO Temperatura no interior da carne: 60ºC Características: Carne diminui de tamanho, o vermelho dá lugar ao cor-de-rosa e as fibras começam a se desnaturalizar. BEM PASSADO Temperatura no interior da carne: 75ºC Características: Carne perdeu 1/6 de seu tamanho e está marrom-acinzentada. O tecido conjuntivo está dissolvido e não há mais líquido para ser liberado. 
Dos 116 elementos químicos presentes na natureza, 14 são essenciais ao equilíbrio nutricional do organismo
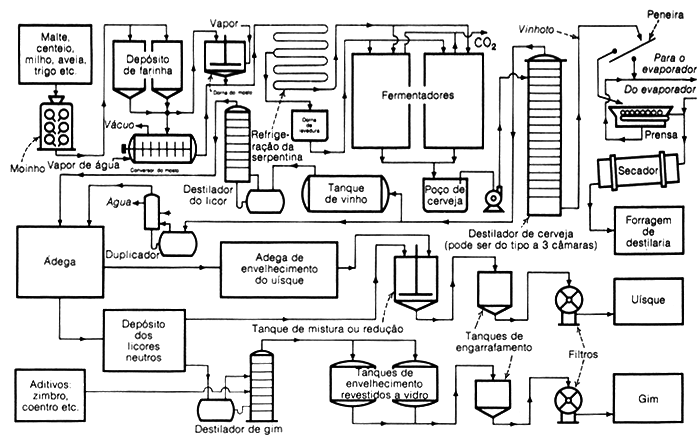
AlambiqueA destilação é uma das operações químicas que a humanidade utiliza há mais tempo. Esse termo vem do latim de-stillare, que pode ser traduzido por gotejar. Existem relatos de que as primeiras destilações teriam sido feitas por chineses, mesopotâmicos e egípcios mesmo antes de 2000 a.C., com o objetivo de obter bálsamos medicinais e essências. Aristóteles, por volta do ano 400 a.C., também menciona a destilação como uma técnica para obter água potável a partir de água do mar. Dos gregos, essa técnica passa aos romanos e depois aos árabes, que criaram um equipamento para destilação empregado até nossos dias: o alambique.O alambique (do árabe al-ambiq, que por sua vez vem do grego ambix, designação de um tipo de vaso com uma abertura pequena) foi desenvolvido por um alquimista árabe chamado Abu Musa Jābir ibn Hayyān, que também é conhecido como “pai da Química”. Ele desenvolveu o alambique no século VIII d.C., provavelmente baseado em equipamentos mais antigos, como o criado por Maria, a Judia (a mesma que criou o banho-maria), famosa química que viveu no Império Romano no século III d.C. Até hoje o alambique é empregado na produção de bebidas destiladas, como a brasileiríssima cachaça, o uísque, a vodca e o absinto – famoso por seu alto teor alcoólico, cujos efeitos fizeram dele a bebida preferida de diversos artistas. Através dessa técnica, é possível aumentar o teor alcoólico das bebidas, já que, na fermentação, teores de etanol acima de 15% levam à morte dos microorganismos fermentadores. Um dos problemas do alambique árabe era a sua baixa capacidade de troca de calor, já que o arrefecimento dos vapores era feito pelo ar circundante do duto de destilação. Esse problema foi resolvido com o desenvolvimento dos condensadores, em que a água, de maior capacidade calorífica, substitui o ar; o condensador de Leibig (condensador de tubo reto) é o descendente direto dos antigos alambiques. O processo envolvido na destilação das bebidas é a destilação por arraste a vapor, na qual os vapores de etanol e água formam uma mistura azeotrópica e carreiam diversos componentes voláteis presentes na bebida fermentada que está sendo submetida ao processo de destilação. Esses componentes podem ser aldeídos, cetonas e ésteres, entre outros, e fazem parte do bouquet da bebida. A esses componentes destilados irão se juntar outros, advindos do processo de envelhecimento em barris, quando a mistura de etanol e água irá extrair componentes da madeira, como acontece na cachaça.
Indicadores de pH naturaisVários vegetais possuem derivados fenólicos cuja cor varia em função do pH do meio, como as antocianinas. Podemos utilizar este fato para obter indicadores de pH naturais.Hoje vamos trabalhar com três vegetais: repolho roxo, uva rubi e tangerina (para as fotos, usamos a do tipo morcote). Corte o repolho roxo em pedaços pequenos e ferva em um pouco de água. Deixe esfriar e coe para tubos de ensaio (3 tubos). Mais tarde, você fará a mesma experiência com as cascas de uva rubi e, ainda depois, com as cascas de tangerina. Ou seja, você usará três tubos para cada vegetal. No caso do repolho roxo, adicione ácido cítrico (que você pode comprar em lojas de perfumaria artesanal) em um dos tubos: observe a mudança de coloração de roxo (pH neutro) para vermelho (pH ácido). No outro tubo, adicione bicarbonato de sódio (que você encontra em qualquer supermercado): a coloração mudará para azul (pH básico).     Sabor Voador
Em 1 hora a Vitamina C desaparece do Suco?
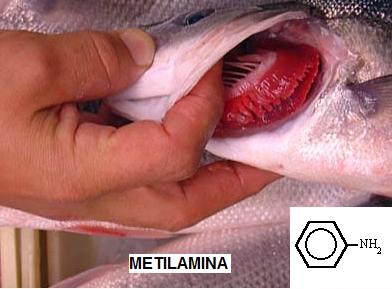
Cheiro de Peixe
Ralador de Queijo tem material Radioativo 
Seu celular tem mais bactérias do que a sola do seu sapato. Fico pensando como o mundo é mais sujo do que a gente imagina, e às vezes bem mais perigoso, como é o caso da chamada desse artigo. Uma empresa de pesquisas revelou que milhares de itens domésticos, de raladores a botões de elevador, têm um nível radioativo mais alto do que o permitido. Isso porque nem todo material radioativo reciclado é testado antes de ser reutilizado. Segundo o estudo, alguns pesquisadores acreditam que o contato com esses metais pode não ser prejudicial, já que até a banana contém material radioativo. Veja a pesquisa aqui.
|
|---|


.jpg)

_Rainha_Nutraceuticos_m.jpg)







.jpg)


.jpg)











Nenhum comentário:
Postar um comentário